
UDI (Unique Device Identifier)
Tra i principali cambiamenti apportati dal nuovo Regolamento UE 2017/745 c’è l’obbligo, da parte del fabbricante, dell’attribuzione del codice UDI (Unique Device Identifier), che ha lo scopo di garantire la tracciabilità dei dispositivi medici lungo tutta la catena di fornitura fino all’utente finale o al paziente e che consentirà di adottare misure rapide ed efficaci in caso di problemi di sicurezza.
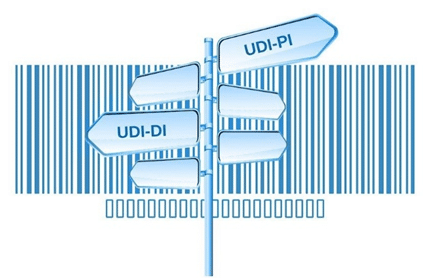
Il codice UDI è costituito da due parti:
- UDI-DI legato al prodotto (che dm è) e viene identificato da un codice numerico o alfanumerico;
- UDI-PI legato alle informazioni di tracciabilità e rintracciabilità del prodotto (numero di lotto, data di scadenza, data di produzione ecc..) ed è anch’esso un codice numerico o alfanumerico.
Tale codice dovrà essere specifico per fabbricante e tipologia di prodotto e dovrà essere apposto sull’etichetta e/o sul confezionamento del dm.
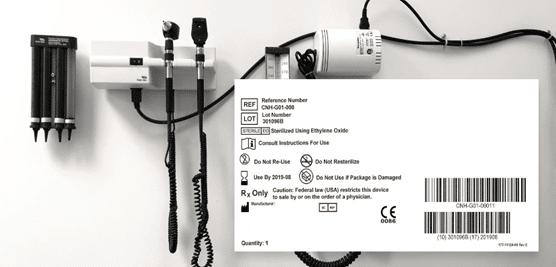
All’interno dell’UE il fabbricante deve assegnare ai suoi dispositivi non solo un identificativo unico, ma anche un UDI-DI di base.
L’UDI-DI di base è l’informazione chiave principale della banca dati e della documentazione pertinente (per esempio certificati, dichiarazione di conformità, documenti tecnici e sintesi delle prestazioni cliniche e di sicurezza) e sarà anche la chiave di accesso alle informazioni sul dispositivo inserite nella futura banca dati europea sui dispositivi medici. L’UDI-DI di base identifica il modello del dispositivo ed è rappresentato da un codice numerico o alfanumerico.
TIMELINE
Gli obblighi relativi all’apposizione da parte del fabbricante del vettore UDI sull’etichetta dei dispositivi medici e su tutti i livelli di confezionamento esterno si applicano secondo le seguenti tempistiche:
- per i dispositivi impiantabili e per i dispositivi appartenente alla classe III dal 26 maggio 2021;
- per i dispositivi appartenenti alle classi IIa e IIb dal 26 maggio 2023;
- per i dispositivi appartenenti alla classe I dal 26 maggio 2025.
Per i dispositivi riutilizzabili che devono recare il vettore UDI sul dispositivo stesso, l’obbligo si applica:
- dal 26 maggio 2023 per i dispositivi impiantabili e per i dispositivi appartenenti alla classe III;
- dal 26 maggio 2025 per i dispositivi appartenenti alle classi IIa e IIb;
- dal 26 maggio 2027 per i dispositivi appartenenti alla classe I.




0 commenti